Senyawa Basa Menurut Bronsted !!
rangkuman teori asam basa menurut arrhenius bronsted lowry.
terdapat teori asam basa yang dikemukakan oleh ahli misalnya.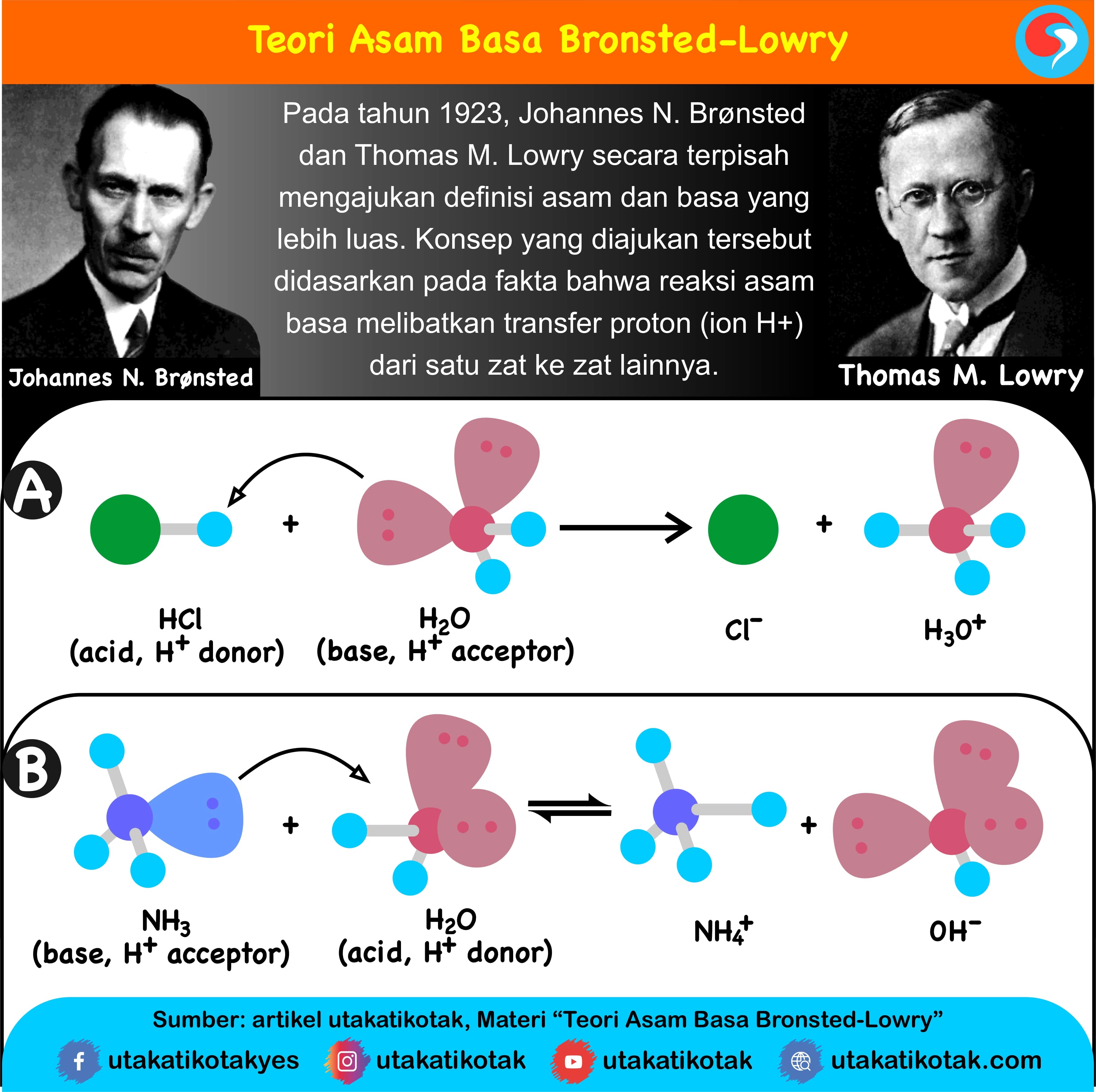
teori asam basa bronsted lowry wikipedia bahasa indonesia.
johannes nicolaus bronsted dan thomas martin lowry secara terpisah memformulasi ide bahwa asam adalah donor proton h sementara basa adalah akseptor proton menurut teori arrhenius asam didefinisikan sebagai senyawa yang jika terdisosiasi di dalam larutan akuatik membebaskan h ion hidrogen.teori asam basa menurut arhennius brosted lowry dan lewis.
06 08 2021 teori asam basa bronsted lowry menjadikan transfer proton h untuk menentukan sifat asam atau basa suatu senyawa definisi asam menurut bronsted lowry adalah zat yang dapat menyumbangkan proton sedangkan basa adalah zat yang dapat menerima proton.
asam basa menurut bronsted lowry.
menurut bronsted dan lowry asam adalah spesi yang memberi proton sedangkan basa adalah spesi yang menerima proton pada suatu reaksi pemindahan proton pengertian asam basa arrhenius hanya berlaku untuk senyawa yang larut dalam pelarut air karena reaksi ionisasi yang menghasilkan ion h dan in oh hanya terjadi dalam pelarut air.pengertian asam dan basa menurut bronsted lowry.
menurut bronsted lowry menyatakan bahwa senyawa hcl bersifat asam karena dalam larutannya menghasilkan ion h sedangkan naoh bersifat basa karena dalam larutannya melepaskan ion oh teori asam basa arrhenius ini berlaku jika dalam keadaan berikut senyawa yang terlibat dalam reaksi harus dalam bentuk larutan.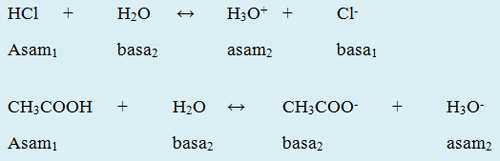
teori asam basa bronsted lowry belajar bersama.
07 12 2015 teori ini disebut teori asam basa bronsted lowry pengertian asam basa bronsted lowry senyawa hcl dalam air bersifat asam karena menurut arrhenius melepaskan ion h tetapi ketika dilarutkan dalam pelarut benzena ternyata sifatnya bukann asam.jelaskan teori asam basa menurut arrhenius bronst.
basa adalah senyawa yang dapat memberikan pasangan elektron bebas peb kepada senyawa lain donor peb contohnya jadi pengertian asam basa menurut teori arrhenius bronsted lowry dan lewis sesuai dengan penjelasan di atas.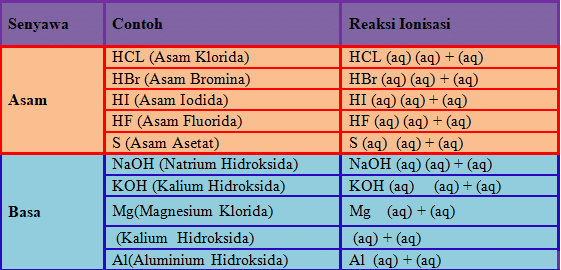
teori asam basa menurut para ahli kelas pintar.
29 12 2020 tidak semua senyawa yang dalam rumus kimianya terdapat gugus hidroksida termasuk golongan basa teori bronsted lowry pada tahun 1923 ahli kimia johannes nicolaus bronsted dan thomas martin lowry mengembangkan definisi asam dan basa berdasarkan kemampuan donor atau menerima akseptor proton ion h.asam basa menurut bronsted lowry siswapedia.
20 02 2020 asam basa menurut bronsted lowry melengkapi kelemahan dari teori arrhenius yang menyatakan bahwa asam merupakan senyawa hidrogen yang jika dilarutkan dalam air akan menghaslkan ion h dalam larutan sedangkan basa adalah suatu senyawa yang bila dilarutkan dalam air akan menghasilkan ion oh dalam larutan namun pada teori arrhenius tidak dapat menjelaskan fakta fakta yang baru ditemukan karena hanya dapat menjelaskan senyawa senyawa dengan rumus kimia ha untuk asam dan loh untuk basa.
teori asam basa arrhenius bronsted lowry lewis amruid.
senyawa asam dan basa sangat mudah dijumpai dalam kehidupan sehari hari misalkan pada senyawa asam dengan ciri khas mempunyai rasa masam contohnya asam cuka vitamin c jeruk nipis dll pada senyawa basa dengan ciri khas mempunyai rasa pahit dan licin bila dipegang contohnya detergen pasta gigi kapur sirih dll.senyawa basa menurut bronsted
senyawa adalah,senyawa aromatik,senyawa anorganik,senyawa air,senyawa alkana,senyawa alkohol,senyawa alkena,senyawa asam,senyawa aromatis,senyawa alifatik,basa adalah,basa arabic,basa artinya,basa arrhenius,basa asam,basa ampek balai,bahasa arab,basa aritonang,basa artinya sunda,basa ammonia,menurut asal katanya porifera berarti,menurut arrhenius asam adalah,menurut arrhenius h2o,menurut arrhenius basa adalah,menurut artinya kalimat imperatif adalah,bronsted acid,bronsted acid and base,bronsted acid definition,bronsted acid examples,bronsted and lowry,bronsted acid and base examples,bronsted acid vs lewis acid,bronsted acid means,bronsted acid and base definition,bronsted acid base reaction


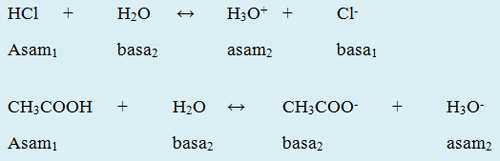

Posting Komentar untuk "Senyawa Basa Menurut Bronsted !!"